Effect of Shugan Yishen Recipe on Microenvironment Gene Expression Profile and Immune-Related Gene Expression in Lung Metastasis of Breast Cancer
-
摘要:目的
通过研究疏肝益肾方对乳腺癌小鼠肺部微环境基因表达的影响,探讨疏肝益肾方抑制乳腺癌肺转移的作用机制。
方法构建乳腺癌原位移植瘤高转移模型,随机分为生理盐水组,疏肝益肾低、中、高(0.5、1、2 g·kg-1)剂量以及多西他赛组(5 mg·kg-1),干预28 d。HE染色观察肺组织结构情况;对转移灶进行转录组分析,通过生物信息学分析基因表达谱的GO和KEGG通路特点,筛选关键差异基因表达情况,采用qPCR和Western blot分析关键免疫基因的表达。流式细胞术检测髓源抑制细胞(Myeloid suppressor cells,MDSCs)表达情况;ELISA法检测细胞因子和趋化因子Cxcl2、GM-CSF的表达。
结果与生理盐水组相比,疏肝益肾方中、高剂量组与多西他赛组肺组织转移结节数量均有相应减少;HE染色提示肺部病理程度有所改善。疏肝益肾方高剂量组与生理盐水组的肺组织微环境有814个差异表达基因,其中713个基因下调,101个基因上调;筛选疏肝益肾组中关键炎性介质基因Nfkbiz、Tnfaip3、Maff、Hspa1a、Hspb1、Cxcl2,与生理盐水组相比,疏肝益肾方组炎性基因显著下调(P < 0.05,P < 0.01),最终其结果与转录组结果趋势相符。采用Western blot在蛋白质层面进行验证,发现与生理盐水组相比,疏肝益肾方组Nfkbiz、Tnfaip3、Maff、Hspa1a和Cxcl2蛋白表达水平下降(P < 0.05,P < 0.01),但Hspb1蛋白表达上调(P < 0.01)。疏肝益肾方组和多西他赛组能够抑制MDSCs表达(P < 0.001),一定程度降低Cxcl2、GM-CSF的表达(P < 0.05,P < 0.01)。
结论疏肝益肾方能抑制乳腺癌肺转移,并且调控肺部免疫微环境基因,其调控范围较广。
Abstract:ObjectiveTo investigate the mechanism of inhibition of breast cancer lung metastasis by Shugan Yishen Recipe by studying the effects of Shugan Yishen Recipe(SGYSR) on gene expression in the lung microenvironment of mice with breast cancer.
MethodsA high metastasis model of breast cancer was constructed, and the mice were randomly divided into saline group, low, medium, high(0.5, 1, 2 g ·kg-1) Shugan Yishen Recipe groups, and docetaxel group (5 mg ·kg-1), and intervened for 28 days. HE staining was used to observe the lung tissue structure; transcriptome analysis was performed on the metastatic foci, and the key differential gene expression was screened by bioinformatics analysis of the GO and KEGG pathway characteristics of the gene expression profiles, and the expression of key immune genes was analyzed by qPCR and Western blot. The expression of MDSCs was detected by flow cytometry; the expression of cytokines and chemokines including Cxcl2, and GM-CSF was detected by ELISA.
RESULTSCompared with the saline group, the number of metastatic nodules in lung tissues of the middle and high dose groups of Shugan Yishen Recipe and docetaxel group were correspondingly lower; HE staining suggested that the degree of lung pathology was improved. There were 814 differentially expressed genes in the lung microenvironment of the high-dose group of Shugan Yishen Recipe and the saline group, of which 713 genes were down-regulated and 101 genes were up-regulated; screening for key inflammatory mediator genes in the Shugan Yishen Recipe group, Nfkbiz, Tnfaip3, Maff, Hspa1a, Hspb1 and Cxcl2, the inflammatory genes in the Shugan Yishen Recipe, as compared with that of the saline group, were significantly down-regulated (P < 0.05, P < 0.01), and ultimately its results were consistent with the trend of the transcriptome results. Western blot was used to verify the results at the protein level, and it was found that compared with the saline group, the protein expression levels of Nfkbiz, Tnfaip3, Maff, Hspa1a and Cxcl2 in the Shugan Yishen Recipe group were decreased(P < 0.05, P < 0.01), while the protein expression of Hspb1 was up-regulated(P < 0.01). Both the Shugan Yishen Recipe group and the docetaxel group could inhibit the expression of MDSCs (P < 0.001), and the expression of Cxcl2, and GM-CSF decreased to a certain extent (P < 0.05, P < 0.01).
CONCLUSIONShugan Yishen Recipe can inhibit breast cancer lung metastasis and regulate the lung immune microenvironment genes in a wide range.
-
乳腺癌(Breast cancer,BRC)在女性的发病率居全球第一,死亡率位居第二[1]。目前,以手术为主的综合治疗是BRC的主要治疗方式,但仍有19%以上患者出现术后3年复发转移,转移性BRC的5年生存率仅14%[2]。因此,高转移率是乳腺癌患者死亡的主要原因,也是亟待解决的医学难题。
《景岳全书·积聚》将肿瘤发生发展的病机总结为“凡脾肾不足及虚弱失调之人,多有积聚之病”[3],另《内经知要》云:“郁者,痞塞不通。”[4]课题组前期流行病学研究发现,乳腺癌患者肝郁证型比例显著高于其他证型,并且肝郁证型与乳腺癌预后不良有显著相关性[5]。因此,本课题组认为脾肾亏虚,正气不行,气郁余毒伏居,癌毒传舍,最终导致肿瘤转移,病位在乳,脾肾亏虚为本,肝郁为标,为本虚标实之证。并基于《素问·六元正纪大论》中“衰其大半而止”的原则,总结出以疏肝益肾填精治法的临床验方-疏肝益肾方,前期研究证实,疏肝益肾方能够改善乳腺癌术后患者骨质疏松、生活质量,调节免疫状态的作用[6-7],但其具体机制尚不清楚。本研究旨从疏肝益肾方对乳腺癌小鼠肺部微环境中的基因表达变化进行分析,为中医药靶向转移前微环境的治疗提供依据。
1. 材料
1.1 动物与细胞株
SPF级Balb/c雌性小鼠,6周龄,购自江苏集萃药康生物科技股份有限公司,动物生产许可证号:SCXK(苏)2023-0009。小鼠饲养于上海市中医医院动物房,适应性饲养1周后予以原位接种乳腺癌细胞。小鼠乳腺癌细胞4T1购自中科院上海生命科学研究院细胞库。本实验经上海市中医医院动物伦理委员会批准,伦理号:2023029。
1.2 实验药物
疏肝益肾方(柴胡18 g, 党参18 g, 半夏18 g, 黄芩9 g, 大枣9 g, 干姜3 g, 菟丝子27 g, 甘草6 g, 煅牡蛎30 g, 紫草15 g)。上述中药饮片均购自上海市中医医院。将上述药材按剂量称取,煎煮后浓缩至含生药量8 g·mL-1,冷却后置于4 ℃冰箱内保存备用。用时稀释成相应浓度用于体内实验。多西他赛(Docetaxel, DTX),规格:50 mg,购自美国MCE公司。
1.3 试剂与抗体
苏木素伊红(HE)染液(货号:C0105S,碧云天);FastPure Cell/Tissue Total RNA Isolation Kit V2试剂盒(货号:RC112-01,诺唯赞);PrimeScriptTM FAST RT reagent Kit with gDNA Eraser试剂盒(货号:RR092A,Takara);TB Green® Premix Ex TaqTM Ⅱ FAST qPCR试剂盒(货号:CN830A,Takara);BCA蛋白定量试剂盒(货号:KGPBCA,凯基生物);Cxcl2、GM-CSF ELISA试剂盒(货号:EM30143M、EM30224M,上海威奥生物科技有限公司);Nfkbiz抗体(货号:14014-1-AP,Proteintech);Tnfaip3抗体(货号:DF6850,Affinity Biosciences);Maff抗体(货号:12771-1-AP,Proteintech);Hspa1a抗体(货号:10995-1-AP,Proteintech);Hspb1抗体(货号:18284-1-AP,Proteintech);CXCL2抗体(货号:ab317569,abcam);Anti-Mouse APC-Cy7 CD45抗体(货号:557659,BD Pharmingen);Anti-Mouse FITC CD11b抗体(货号:557396,BD Pharmingen);Anti-Mouse PE Ly-6G and Ly-6C抗体(货号:553128,BD Pharmingen)。
1.4 仪器
371型CO2细胞培养箱(Thermo Fisher Scientific);Veriti Dx96核酸扩增仪(ABI公司);CFX96荧光定量PCR[伯乐生命医学产品(上海)有限公司];DYY-6C型蛋白垂直电泳仪(北京市六一仪器厂);ChemiDoc XRS+化学发光成像系统[伯乐生命医学产品(上海)有限公司];CytoFLEX流式细胞仪(贝克曼库尔特有限公司)。
2. 方法
2.1 细胞培养
4T1细胞培养在含10%胎牛血清的1640培养基中,置于37 ℃,5%CO2的细胞孵箱中培养。次日更换培养液,待细胞生长融合至70%~80%,用含EDTA的胰酶消化并进行传代。
2.2 动物分组及造模
选取Balb/c雌性小鼠40只随机分为生理盐水组,疏肝益肾方低、中、高剂量组,多西他赛组,每组8只。适应性喂养1周后构建原位移植瘤转移模型。取对数生长期的乳腺癌4T1细胞,PBS稀释成2.5×106 mL-1单细胞悬液。按照每只200 μL(5×105个)接种于小鼠第4对乳腺脂肪垫,后继续饲养28 d。
2.3 给药
根据成人和小鼠等效剂量换算[8],中药干预低、中、高剂量组小鼠灌胃给予0.5、1、2 g·kg-1疏肝益肾方,多西他赛组给予5 mg·kg-1药物,生理盐水组小鼠灌胃给予生理盐水,给药体积均为0.2 mL,连续给药28 d。
2.4 评估小鼠肺转移情况
实验终点处死小鼠,解剖收获小鼠肺脏,并以Bouin’s液固定24 h后,观察小鼠肺组织表面有无肉眼可见转移灶,不计大小。统计每组小鼠发生肺转移数。
2.5 HE染色观察肺组织病理学变化
将肺组织于福尔马林中固定,脱蜡后切片。于二甲苯和梯度酒精中脱蜡水化,苏木素、伊红染色后水洗,经脱水透明、封片后,采集样本图片。
2.6 转录组测序
利用Illumina高通量测序对乳腺癌小鼠转移肺组织进行转录组测序,分析转移灶相关基因的变化情况。
2.7 肺部免疫微环境差异表达基因功能分析
对生理盐水组和疏肝益肾方组间的差异基因进行GO、KEGG富集分析,分析差异基因主要影响的功能,以便进行后续研究。
2.8 qPCR检测免疫相关基因mRNA的表达
使用RNA提取试剂盒提取总RNA并检测其浓度;qPCR试剂盒将待测RNA逆转录成cDNA,反转录体系如下:5×PrimeScript RT Master Mix 4 μL;8× gDNA Eraser Premix 2 μL;总RNA 1 μg;RNase Free H2O加至20 μL。反应程序如下:37 ℃ 10 min;85 ℃ 5 s。最后使用荧光定量试剂盒在PCR仪上进行检测,体系如下:2× PerfectStart Green qPCR SuperMix, 5 μL; 10 μmol·L-1 Universal primer,0.8 μL;cDNA 2 μL;Nuclease-free H2O 6.4 μL;程序为:95 ℃ 30 s;94 ℃ 5 s,60 ℃ 10 s,40个循环。检测荧光信号,采用2-△△Ct法进行计算并统计表达量。引物信息见表 1。
表 1 各基因引物信息Table 1. Primer information for each genePrimer Forward(5’➝3’) Reverse(3’➝5’) β-actin TATGCTCTCCCTCACGCCATCC GTCACGCACGATTTCCCTCTCAG Nfkbiz CGCTCAACCTGGCTTACTTCTACG AAGTGGAGGAGAAATCGGAGGAGTC Tnfaip3 CTGTCACCAACGCTCCAAGTCTG TGCTTGTCCCTGCTCTGTCTCC Maff AGCAAAGCCCTGAAGGTCAAGC GTCACCTCCTCCGCCGACAG Hspa1a GGTGCTGACGAAGATGAAGGAGATC CTGCCGCTGAGAGTCGTTGAAG Hspb1 GCTCACAGTGAAGACCAAGGAAGG GCACCGAGAGATGTAGCCATGTTC Cxcl2 CACTGGTCCTGCTGCTGCTG GCGTCACACTCAAGCTCTGGATG 2.9 Western blot检测
将适量肺组织裂解后,12 000 r·min-1,4 ℃,离心15 min,取上清,并用BCA测定蛋白质含量。制备下层胶,待下层胶凝固后加入上层胶并插入梳子。倒入适量电泳缓冲液后开始上样,每孔20 μg蛋白。浓缩胶80 V,30 min,分离胶120 V,60 min,进行电泳。转膜条件为300 mA,60 min。5%脱脂奶粉封闭后一抗4 ℃孵育过夜。二抗室温孵育1 h,均匀蘸取已配置好的ECL发光液后,于成像系统中进行扫描并采集图像。
2.10 流式细胞术检测
制备肺组织单细胞混悬液,加入相应流式抗体进行染色:APC-Cy7-CD45、FITC-CD11b、PE-Gr-1,室温避光孵育15 min后加入PBS洗涤,待上机检测。
2.11 ELISA检测
依据ELISA试剂盒说明书检测小鼠肺组织中相关免疫因子Cxcl2、GM-CSF的水平。
2.12 统计学方法
所有统计分析均使用SPASS。收集的各组数据用x±s表示。多组间的比较采用ANOVA方差分析。两组间的比较采用独立样本t检验。P<0.05为差异有统计学意义。
3. 结果
3.1 疏肝益肾方抑制4T1乳腺癌小鼠肺转移率
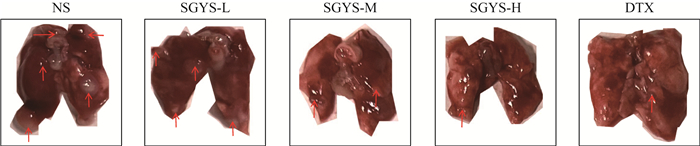
本研究通过构建乳腺癌肺转移模型,观察各组小鼠肺转移情况。结果显示(见图 1,表 2),与生理盐水组相比,疏肝益肾方低剂量组无明显抑制肺转移的作用(P>0.05),中、高剂量以及多西他赛组均能降低乳腺癌小鼠肺组织转移结节数量(P < 0.05,P < 0.01,P < 0.001),其中疏肝益肾方高剂量组和多西他赛组抑制肺转移作用相当。
表 2 各组小鼠肺转移病灶结节数Table 2. The number of nodules in lung metastatic lesions in mice of each group组别 剂量/(g·kg-1) 肿瘤结节数 生理盐水组 — 6.20±1.79 疏肝益肾方低剂量组 0.5 6.00±1.58 疏肝益肾方中剂量组 1.0 3.80±0.84* 疏肝益肾方高剂量组 2.0 3.00±0.71** 多西他赛组 0.005 2.20±0.84*** 注:与生理盐水组比较,*P < 0.05,**P < 0.01,***P < 0.001。 3.2 疏肝益肾方抑制乳腺癌小鼠肺组织病理改变
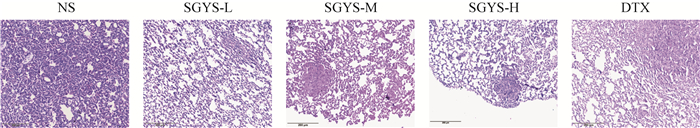
采用HE染色明确各组小鼠肺组织病理结构情况。结果如图 2显示,与生理盐水组相比,疏肝益肾方组和多西他赛组小鼠肺组织中的肺泡结构紊乱程度、炎症细胞浸润程度均有不同程度的改善,表明疏肝益肾方可以减轻乳腺癌肺转移小鼠肺组织的炎症及转移灶情况。
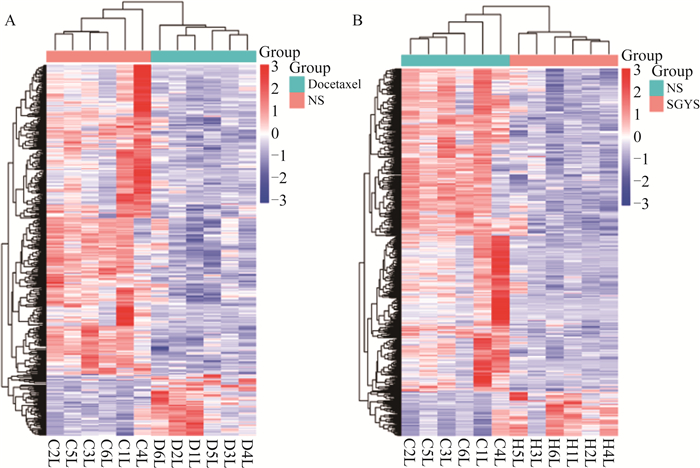
3.3 不同治疗组肺转移灶差异基因表达谱比较
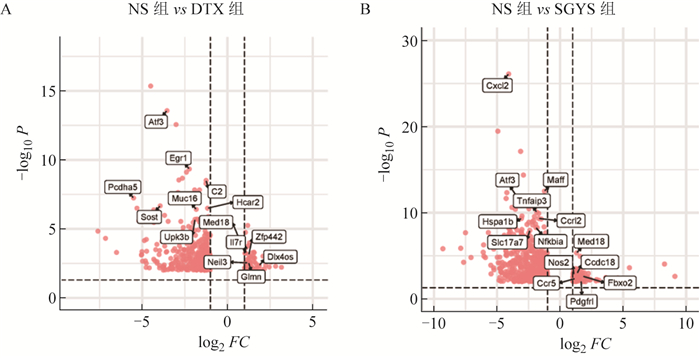
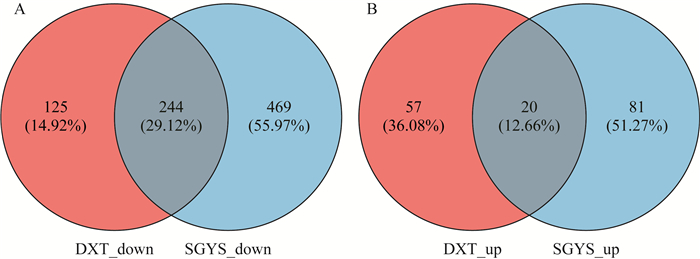
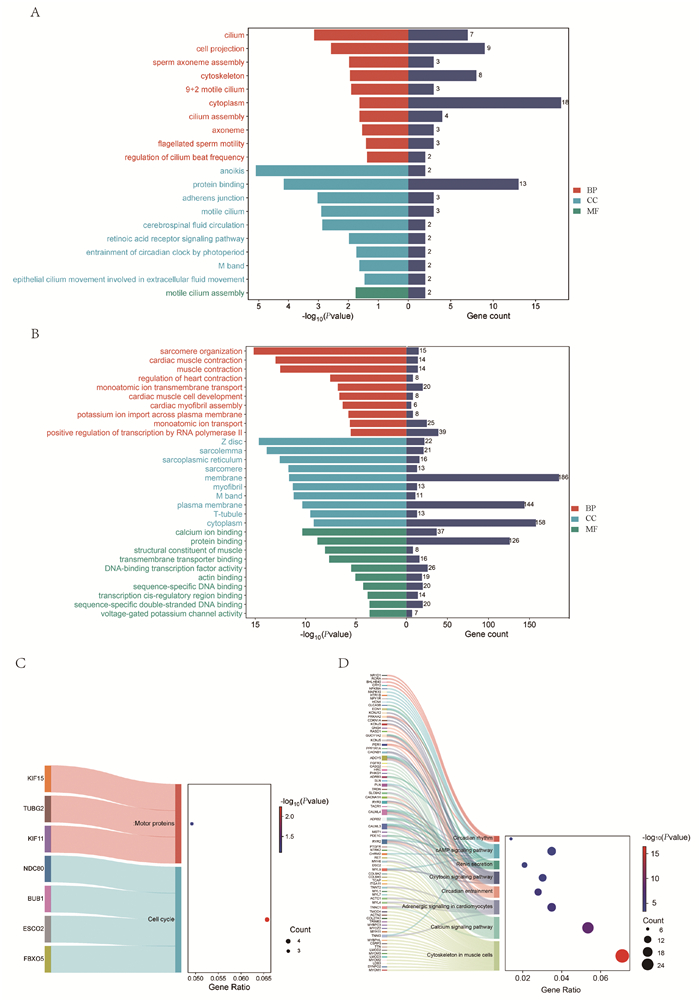
将各组表达基因与生理盐水组相比,以P < 0.01和|Log2FC|>2为筛选条件,结果显示:多西他赛组共有446个差异基因,其中包括77个上调基因和369个下调基因;疏肝益肾方组差异基因数远高于多西他赛组,共有814个差异基因,其中包括101个上调基因和713个下调基因(见图 3~4)。与生理盐水组相比,多西他赛组上调基因前5位基因是:Muc2、Lrrc75b、Zfp971、Med18、Zfp442,基因表达下调的前5位基因是:Il6、Egr1、Has1、C2、Phlda3;SGYS组上调基因前5位基因是:Med18、Prnd、Gpnmb、Nusap1、Mis18bp1,基因表达下调的前5位基因为:Cxcl2、Fosb、Hspb1、Maff、Hrc。另外,Hspa1a、Tnfaip3和Nfkbiz差异基因分别排在下调差异基因的第6位、第11位和第14位。在差异基因中,疏肝益肾方组与多西他赛组共有264个相同差异基因,其中有20个基因共同上调,244个基因共同下调(见图 5)。
3.4 不同治疗组肺转移灶差异表达基因GO富集分析比较
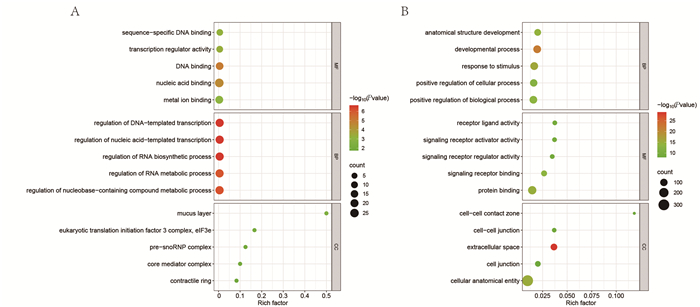
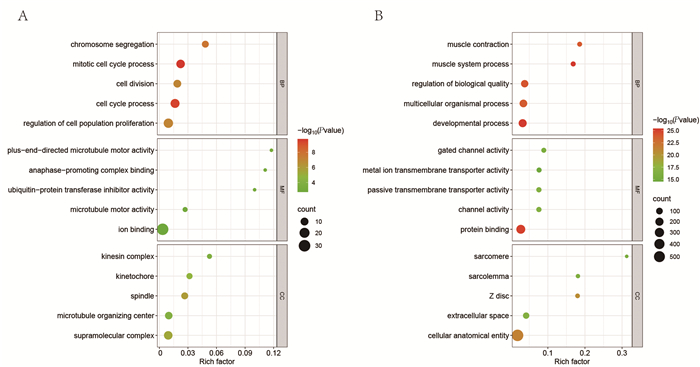
分别对多西他赛组、疏肝益肾方组差异表达上调和下调基因进行GO富集分析,结果显示:多西他赛组下调差异基因与生物过程(Biological process,BP)相关的GO条目有21条,主要集中在发育过程和应激反应上;细胞组分(Cell components,CC)有14条,主要富集在细胞结构域和细胞连接功能上;分子功能(Molecular function,MF)有12条,主要分布在信号受体激活和连接功能上;多西他赛组表达上调的差异基因GO聚类主要富集在转录因子激活、DNA连接及RNA代谢调节过程等功能(图 6)。疏肝益肾方组上调差异基因GO富集分析,得到生物过程条目17条,主要集中在解剖结构发育及对刺激响应功能上,细胞组成条目12条,多与受体活性及蛋白质结合相关,分子功能条目7条,主要富集在细胞-细胞连接区及细胞外分泌功能上;而疏肝益肾方下调差异基因GO聚类与多西他赛组下调基因在发育过程、生物系统进程调控功能类似,并富集在免疫系统过程和代谢过程上。以上结果提示疏肝益肾方对乳腺癌肺组织微环境的生物学过程的调控可能与多西他赛相似(见图 7)。
3.5 不同治疗组肺转移灶差异表达基因KEGG信号通路富集比较
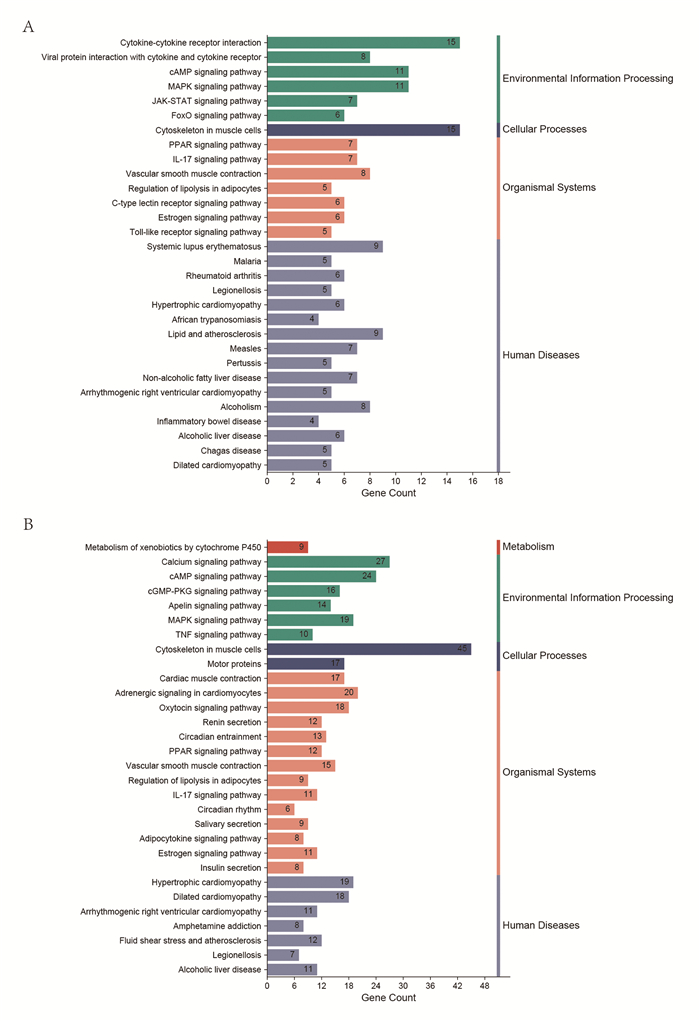
在明确疏肝益肾方和多西他赛调控小鼠肺组织微环境的GO富集聚类情况后,我们进一步分析差异基因KEGG通路富集情况。多西他赛组77个上调差异基因注释到的KEGG通路共2条,其中满足FDR < 0.05的通路1条:Ribosome biogenesis in eukaryotes(path:mmu03008)。369个下调差异基因注释到KEGG通路共计32条,其中P < 0.05且FDR < 0.05的通路共1条:Cytoskeleton in muscle cells(path:mmu04820)。疏肝益肾方组101个上调差异基因注释到KEGG通路共2条,其中满足FDR < 0.05的通路0条。下调基因注释到KEGG通路共计56条,其中P < 0.05且FDR < 0.05的通路共18条,包括Calcium signaling pathway(path:mmu04020),cAMP signaling pathway(path:mmu04024),IL-17 signaling pathway(path:mmu04657)等。随后,我们以P < 0.05为筛选条件分别对KEGG途径(Top30)进行分类,结果显示(见图 8),多西他赛组富集的KEGG途径分为4类:环境信息处理,细胞途径过程,生物系统和人类疾病;疏肝益肾方组注释的KEGG途径聚类在代谢、环境信息处理,细胞途径过程,生物系统和人类疾病。以上提示疏肝益肾方对乳腺癌小鼠肺组织微环境的调控机制与多西他赛有共性,但疏肝益肾方涉及的通路范围更为广泛。
3.6 疏肝益肾方对肺转移灶特异表达基因的生物信息学分析
本研究进一步对疏肝益肾方组中81个特异性表达上调基因和469个特异性表达下调的基因进行GO和KEGG pathway富集分析(见图 9)。特异性上调基因GO功能主要包括:细胞骨架、视黄酸受体信号通路和光周期对生物钟的影响等。特异性下调基因GO功能主要包括:心肌细胞发育、RNA聚合酶转录的正向调控及钙离子结合蛋白等。特异性上调基因注释的KEGG pathway主要包括:cell cycle(pathway:mmu04110),参与调控细胞周期,其中通路相关基因有Fbxo5、Esco2、Bub1、Ndc80。特异性下调基因富集的KEGG pathway主要包括钙信号通路、肾素分泌及昼夜节律信号通路等,主要相关基因包括Per1、Rora、Ret、Edn1等。
3.7 疏肝益肾方对肺转移微环境中炎性介质表达的影响
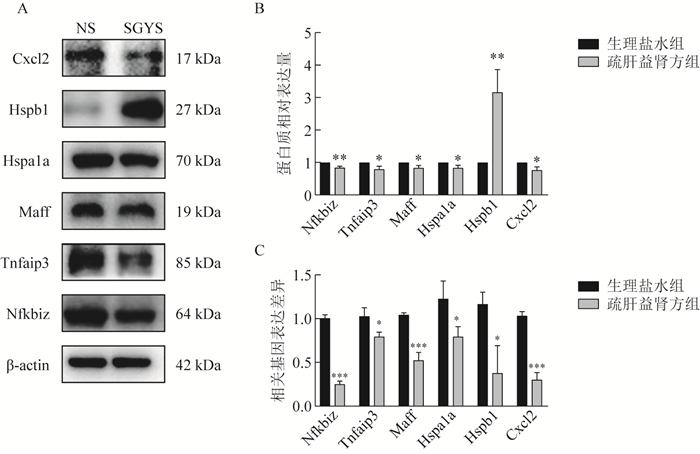
根据课题组前期研究发现,疏肝益肾方防治乳腺癌转移的作用与炎性微环境密切相关。根据GO、KEGG的富集结果对差异基因进行分析,筛选出Nfkbiz、Tnfaip3、Maff、Hspa1a、Hspb1、Cxcl2基因。随后,我们采用qPCR验证肺组织中炎性介质的表达变化,结果发现与生理盐水组相比,疏肝益肾方组中Nfkbiz、Tnfaip3、Maff、Hspa1a、Hspb1和Cxcl2表达下降(P < 0.05,P < 0.01),与基因表达谱芯片结果一致,其中Nfkbiz和Cxcl2下降最为显著(P < 0.001)。同时,我们采用Western blot在蛋白质层面进行验证,结果显示(图 10),与生理盐水组相比,疏肝益肾方组Nfkbiz、Tnfaip3、Maff、Hspa1a和Cxcl2蛋白表达水平下降(P < 0.05,P < 0.01),与mRNA一致,但Hspb1蛋白表达上调(P < 0.01)。由此可见,疏肝益肾方可以下调Nfkbiz、Tnfaip3、Maff、Hspa1a和Cxcl2基因和蛋白的表达,对Hspb1表达的影响还需进一步分析。
3.8 疏肝益肾方调控肺转移组织中MDSCs及其相关炎性因子浸润
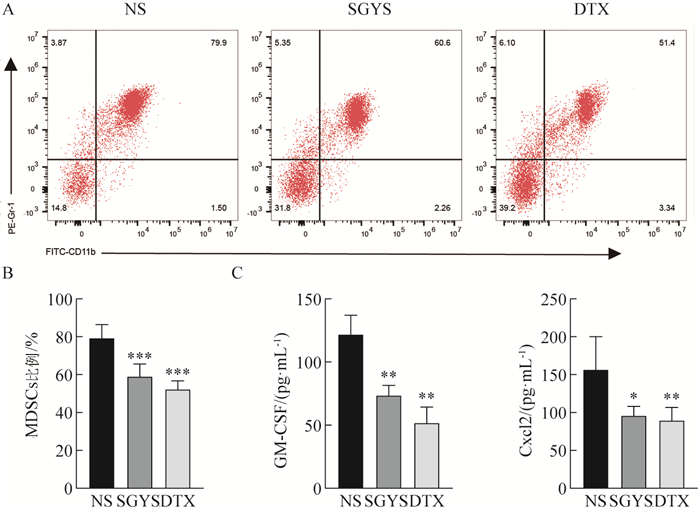
课题组前期研究已证实炎性介质促进免疫抑制微环境形成,并且MDSCs是介导免疫抑制信号的关键环节。本研究采用流式细胞术检测小鼠肺组织中MDSCs比例,结果见图 11,与生理盐水组相比,疏肝益肾方组和多西他赛组均能降低CD11b+Gr-1+细胞比例(P < 0.001);通过ELISA法检测相关炎性因子和趋化因子表达,与生理盐水组相比,疏肝益肾方组和多西他赛组GM-CSF、Cxcl-2表达降低(P < 0.05,P < 0.01),2组间相比无显著性差异,提示炎性介导的免疫微环境重塑可能是疏肝益肾方发挥抗乳腺癌转移的机制之一。
![]() 图 11 疏肝益肾方对乳腺癌肺转移小鼠肺组织中免疫细胞及炎性因子的影响注: A~B.疏肝益肾方对肺组织中MDSCs表达的影响; C.ELISA对肺组织中GM-CSF、Cxcl-2表达的影响。NS.生理盐水组;SGYS.疏肝益肾方组;DTX.多西他赛组。与生理盐水组比较,*P < 0.05, **P < 0.01,***P < 0.001。Figure 11. Effects of Shugan Yishen Recipe on immune cells and inflammatory factors in lung tissues of mice with lung metastases from breast cancer
图 11 疏肝益肾方对乳腺癌肺转移小鼠肺组织中免疫细胞及炎性因子的影响注: A~B.疏肝益肾方对肺组织中MDSCs表达的影响; C.ELISA对肺组织中GM-CSF、Cxcl-2表达的影响。NS.生理盐水组;SGYS.疏肝益肾方组;DTX.多西他赛组。与生理盐水组比较,*P < 0.05, **P < 0.01,***P < 0.001。Figure 11. Effects of Shugan Yishen Recipe on immune cells and inflammatory factors in lung tissues of mice with lung metastases from breast cancer4. 讨论
乳腺癌在祖国医学中归属于“乳岩”“乳石痈”等范畴,肝失疏泄,气机不畅是乳腺癌发病的关键病机。研究显示,情志抑郁程度与癌症患者炎症反应之间存在显著正相关性[9]。乳腺癌转移涉及多种机制[10],包括免疫逃逸、上皮间质转化、血管新生和细胞外基质降解等。其中,一种由肿瘤中的致癌突变决定的持续性炎症状态,是促进癌症进展到转移微环境形成阶段的标志[11]。持续性的炎症一方面直接通过细胞因子信号传导,另一方面通过氮物质和活性氧间接诱导表观遗传修饰,从而导致肿瘤转移[12]。此外,这种“低级别”炎症导致的癌细胞增殖和存活,促进血管生成,破坏适应性免疫反应,导致免疫细胞转化为免疫抑制表型[13]。研究显示,促炎因子IL-23和IL-12之间的平衡稳态,以及MDSCs和效应淋巴细胞之间的比例,与肿瘤免疫逃逸显著相关[14]。另有研究显示,T细胞中NF-κB激活刺激效应T细胞活化,并促进表现为免疫抑制活性的IFN-γ+CD8+T细胞的数量[15]。课题组前期研究也证实,早期肺癌术后患者外周血中IL-1β水平增高,并通过NF-κB通路促进MDSCs免疫抑制活性,影响患者无进展生存期[16]。针对炎性转移前微环境的治疗,对从“治未病”角度防治乳腺癌这一临床问题的解决具有实际意义。
中医药治疗已经在乳腺癌综合治疗中显露出独特优势。课题组在小柴胡汤基础上,加减化裁总结出疏肝健脾、益肾填精的疏肝益肾方。已有研究显示,小柴胡汤能够通过TLR4/MyD88/NF-κB通路降低脓毒血症小鼠血清中NO及TNF-α水平[17]。此外,柴胡皂苷D,作为柴胡的主要小分子化合物,已被证实能够通过抑制β-catenin及下游靶基因诱导三阴性乳腺癌细胞凋亡,发挥抗肿瘤作用[18]。菟丝子和牡蛎为调和肾阴、肾阳常用药对,具有补肾壮阳、补益肝肾、固精缩尿的功效。现代研究显示菟丝子能减少H2O2诱导的氧化损伤,并通过激活PI3K/AKT通路发挥抗炎作用[19]。牡蛎能够通过有氧糖酵解重编程调控肿瘤微环境[20]。
本研究通过建立乳腺癌高转移模型,明确了疏肝益肾方能够抑制乳腺癌肺转移率,并改善肺组织的病理状态。通过对肺组织基因谱分析发现,疏肝益肾方对乳腺癌小鼠肺组织微环境涉及的BP、CC、MF更为广泛,并且筛选出Hspb1、Hspa1a、Maff、Tnfaip3、Cxcl2等基因下调。热休克蛋白β-1(Hspb1)和诱导型70 kDa热休克蛋白(Hspa1a)是人类小热休克蛋白(HSPBs)的成员,与乳腺癌的预后不良相关[21]。其中Hspb1与Ikβ-α结合并促进其泛素化介导的降解,导致核转位增加和NF-κB信号的激活,是其促进乳腺癌进展的机制之一[22]。Hspa1a在乳腺癌患者的血清水平大大升高[23],与本研究结果一致,但具体机制尚不清楚。Maff是与炎症相关的转录因子,在体内和体外均能够作为缺氧基因增强肿瘤细胞的侵袭促进疾病的发展[24];此外,Maff被发现可以作为促炎因子刺激LPS[25]。Tnfaip3被证实在FGFR 1的调节下能够促进乳腺癌小鼠的肿瘤生长以及肺转移,Tnfaip3的敲低可抑制乳腺癌细胞中VEGFA的表达[26]。Cxcl2是CXC家族的一员,作为原癌基因编码的蛋白,可促进血管形成[27],另有研究显示,Cxcl2激活乳腺癌细胞中NOTCH1/HEY1通路可能是维持乳腺癌干性的机制之一[28]。肺组织基因表达谱聚焦于乳腺癌小鼠肺转移微环境,炎性介质是免疫抑制微环境形成的基础,免疫抑制细胞是促进肿瘤免疫逃逸的关节环节[29]。其中,MDSCs是抑制微环境形成的主要角色,MDSCs耗竭能够抑制乳腺癌细胞的迁移与侵袭[30]。此外,免疫微环境中存在细胞因子和趋化因子与免疫细胞间相互作用能够影响肿瘤发生发展。研究显示,肿瘤细胞分泌的GM-CSF能诱导MDSCs扩增[31];趋化因子Cxcl2对MDSCs募集有特异性功能[32],靶向抑制Cxcl2及其受体能够抑制肿瘤中的血管生成和转移。
综上所述,本研究采用乳腺癌转移模型,利用基因芯片技术重点探究疏肝益肾方对乳腺癌肺转移微环境基因组表达的影响,结果显示疏肝益肾方可以干预多种炎性介质基因的表达,并且相关显著差异基因涉及免疫调节、心肌细胞发育等生物功能,以及参与更为广泛的通路调控,如钙信号通路、肾素分泌及昼夜节律信号通路及IL-17信号通路等。此外,Hspb1、Hspa1a、Maff、Tnfaip3、Cxcl2等炎性介质基因表达下调,并且参与调控MDSCs介导的免疫微环境重塑,这可能是疏肝益肾方发挥抗乳腺癌转移的关键靶标。该研究具有重要探索意义,为后续进一步实验明晰了新的方向。
-
图 11 疏肝益肾方对乳腺癌肺转移小鼠肺组织中免疫细胞及炎性因子的影响
注: A~B.疏肝益肾方对肺组织中MDSCs表达的影响; C.ELISA对肺组织中GM-CSF、Cxcl-2表达的影响。NS.生理盐水组;SGYS.疏肝益肾方组;DTX.多西他赛组。与生理盐水组比较,*P < 0.05, **P < 0.01,***P < 0.001。
Figure 11. Effects of Shugan Yishen Recipe on immune cells and inflammatory factors in lung tissues of mice with lung metastases from breast cancer
表 1 各基因引物信息
Table 1 Primer information for each gene
Primer Forward(5’➝3’) Reverse(3’➝5’) β-actin TATGCTCTCCCTCACGCCATCC GTCACGCACGATTTCCCTCTCAG Nfkbiz CGCTCAACCTGGCTTACTTCTACG AAGTGGAGGAGAAATCGGAGGAGTC Tnfaip3 CTGTCACCAACGCTCCAAGTCTG TGCTTGTCCCTGCTCTGTCTCC Maff AGCAAAGCCCTGAAGGTCAAGC GTCACCTCCTCCGCCGACAG Hspa1a GGTGCTGACGAAGATGAAGGAGATC CTGCCGCTGAGAGTCGTTGAAG Hspb1 GCTCACAGTGAAGACCAAGGAAGG GCACCGAGAGATGTAGCCATGTTC Cxcl2 CACTGGTCCTGCTGCTGCTG GCGTCACACTCAAGCTCTGGATG 表 2 各组小鼠肺转移病灶结节数
Table 2 The number of nodules in lung metastatic lesions in mice of each group
组别 剂量/(g·kg-1) 肿瘤结节数 生理盐水组 — 6.20±1.79 疏肝益肾方低剂量组 0.5 6.00±1.58 疏肝益肾方中剂量组 1.0 3.80±0.84* 疏肝益肾方高剂量组 2.0 3.00±0.71** 多西他赛组 0.005 2.20±0.84*** 注:与生理盐水组比较,*P < 0.05,**P < 0.01,***P < 0.001。 -
[1] SIEGEL R L, GIAQUINTO A N, JEMAL A. Cancer statistics, 2024[J]. Cancer J Clin, 2024, 74(1): 12-49. DOI: 10.3322/caac.21820
[2] GIAQUINTO A N, SUNG H, NEWMAN L A, et al. Breast cancer statistics 2024[J]. Cancer J Clin, 2024, 74(6): 477-495. DOI: 10.3322/caac.21863
[3] 张介宾. 景岳全书[M]. 北京: 人民卫生出版社, 2007. ZHANG J B. The complete works of Zhang Jingyue[M]. Beijing: People's Medical Publishing House, 2007.
[4] 李中梓. 内经知要[M]. 北京: 中国医药科技出版社, 2011. LI Z Z. Essential knowledge of internal medicine[M]. Beijing: China Medical Science Press, 2011.
[5] 金岚, 屠思远, 褚美玲, 等. 从气质特征角度看乳腺癌的肝郁属性[J]. 新中医, 2024, 56(7): 195-200. JIN L, TU S Y, CHU M L, et al. Study on liver depression attribute of breast cancer from perspective of temperaments[J]. New Chin Med, 2024, 56(7): 195-200.
[6] 郑诗芸, 崔闯, 陈皖晴, 等. 疏肝益肾方治疗肝郁脾虚型绝经后雌激素受体阳性乳腺癌术后患者的临床疗效[J]. 医学研究杂志, 2024, 53(9): 117-121. ZHENG S Y, CUI C, CHEN W Q, et al. Clinical effects of Shugan yishen recipe on postmenopausal estrogen receptor-positive breast cancer patients with hepatic stagnation and spleen deficiency type[J]. J Med Res, 2024, 53(9): 117-121.
[7] 朱为康, 陈旻, 李雁, 等. 补肾疏肝联合芳香化酶抑制剂治疗绝经后激素受体阳性乳腺癌[J]. 世界中医药, 2020, 15(20): 3113-3116, 3120. ZHU W K, CHEN M, LI Y, et al. Chinese medicine of tonifying kidney and soothing liver qi combined with aromatase inhibitor in the treatment of postmenopausal women with hormone receptor positive breast cancer[J]. World Chin Med, 2020, 15(20): 3113-3116, 3120.
[8] 黄继汉, 黄晓晖, 陈志扬, 等. 药理试验中动物间和动物与人体间的等效剂量换算[J]. 中国临床药理学与治疗学, 2004, 9(9): 1069-1072. HUANG J H, HUANG X H, CHEN Z Y, et al. Dose conversion among different animals and healthy volunteers in pharmacological study[J]. Chin J Clin Pharmacol Ther, 2004, 9(9): 1069-1072.
[9] ANDERSEN B L, MYERS J, BLEVINS T, et al. Depression in association with neutrophil-to-lymphocyte, platelet-to-lymphocyte, and advanced lung cancer inflammation index biomarkers predicting lung cancer survival[J]. PLoS ONE, 2023, 18(2): e0282206. DOI: 10.1371/journal.pone.0282206
[10] ALTEA-MANZANO P, DOGLIONI G, LIU Y W, et al. A palmitate-rich metastatic niche enables metastasis growth via p65 acetylation resulting in pro-metastatic NF-κB signaling[J]. Nat Cancer, 2023, 4(3): 344-364. DOI: 10.1038/s43018-023-00513-2
[11] HANAHAN D. Hallmarks of cancer: New dimensions[J]. Cancer Discov, 2022, 12(1): 31-46. DOI: 10.1158/2159-8290.CD-21-1059
[12] MANTOVANI A, ALLAVENA P, SICA A, et al. Cancer-related inflammation[J]. Nature, 2008, 454(7203): 436-444. DOI: 10.1038/nature07205
[13] DIAKOS C I, CHARLES K A, MCMILLAN D C, et al. Cancer-related inflammation and treatment effectiveness[J]. Lancet Oncol, 2014, 15(11): e493-503. DOI: 10.1016/S1470-2045(14)70263-3
[14] CHRISTOFIDES A, STRAUSS L, YEO A, et al. The complex role of tumor-infiltrating macrophages[J]. Nat Immunol, 2022, 23(8): 1148-1156. DOI: 10.1038/s41590-022-01267-2
[15] UHL L F K, CAI H, ORAM S L, et al. Interferon-γ couples CD8+ T cell avidity and differentiation during infection[J]. Nat Commun, 2023, 14(1): 6727. DOI: 10.1038/s41467-023-42455-4
[16] ZHANG S F, CHEN W Q, WANG Y L, et al. Chinese herbal prescription fu-Zheng-qu-Xie prevents recurrence and metastasis of postoperative early-stage lung adenocarcinoma: A prospective cohort study followed with potential mechanism exploration[J]. Oxid Med Cell Longev, 2021, 2021: 6673828. DOI: 10.1155/2021/6673828
[17] YANG Q X, WANG Y L, CAO G F, et al. Anti-sepsis effect of Xiaochaihu decoction based on the TLR4/MyD88/NF-κB signalling pathway[J]. Heliyon, 2024, 10(5): e26712. DOI: 10.1016/j.heliyon.2024.e26712
[18] WANG J X, QI H, ZHANG X L, et al. Saikosaponin D from Radix Bupleuri suppresses triple-negative breast cancer cell growth by targeting β-catenin signaling[J]. Biomed Pharmacother, 2018, 108: 724-733. DOI: 10.1016/j.biopha.2018.09.038
[19] LIANG Y S, SHI Y, GUO R, et al. Wine- and stir-frying processing of Cuscutae Semen enhance its ability to alleviate oxidative stress and apoptosis via the Keap 1-Nrf2/HO-1 and PI3K/AKT pathways in H2O2-challenged KGN human granulosa cell line[J]. BMC Complement Med Ther, 2024, 24(1): 189. DOI: 10.1186/s12906-024-04491-5
[20] CORPOREAU C, HUVET A, PICHEREAU V, et al. The oyster Crassostrea gigas, a new model against cancer[J]. Med Sci, 2019, 35(5): 463-466.
[21] HUO Q, WANG J, XIE N. High HSPB1 expression predicts poor clinical outcomes and correlates with breast cancer metastasis[J]. BMC Cancer, 2023, 23(1): 501.
[22] LIANG Y R, WANG Y J, ZHANG Y, et al. HSPB1 facilitates chemoresistance through inhibiting ferroptotic cancer cell death and regulating NF-κB signaling pathway in breast cancer[J]. Cell Death Dis, 2023, 14(7): 434.
[23] DE FREITAS G B, PENTEADO L, MIRANDA M M, et al. The circulating 70 kDa heat shock protein (HSPA1A) level is a potential biomarker for breast carcinoma and its progression[J]. Sci Rep, 2022, 12(1): 13012.
[24] MOON E J, MELLO S S, LI C G, et al. The HIF target MAFF promotes tumor invasion and metastasis through IL11 and STAT3 signaling[J]. Nat Commun, 2021, 12(1): 4308.
[25] WANG W, LIU Y, XIONG L L, et al. Synthesis of lathyrol PROTACs and evaluation of their anti-inflammatory activities[J]. J Nat Prod, 2023, 86(4): 767-781.
[26] GAO M D, LI X, YANG M, et al. TNFAIP3 mediates FGFR1 activation-induced breast cancer angiogenesis by promoting VEGFA expression and secretion[J]. Clin Transl Oncol, 2022, 24(12): 2453-2465.
[27] ZHANG R, DONG M X, TU J, et al. PMN-MDSCs modulated by CCL20 from cancer cells promoted breast cancer cell stemness through CXCL2-CXCR2 pathway[J]. Signal Transduct Target Ther, 2023, 8(1): 97.
[28] LIN X Y, ZHAO Z F, CAI Y Q, et al. MyD88 deficiency in mammary epithelial cells attenuates lipopolysaccharide (LPS)-induced mastitis in mice[J]. Biochem Biophys Res Commun, 2024, 739: 150569.
[29] VEGLIA F, SANSEVIERO E, GABRILOVICH D I. Myeloid-derived suppressor cells in the era of increasing myeloid cell diversity[J]. Nat Rev Immunol, 2021, 21(8): 485-498.
[30] EUM D Y, JEONG M, PARK S Y, et al. AM-18002, a derivative of natural anmindenol A, enhances radiosensitivity in mouse breast cancer cells[J]. PLoS ONE, 2024, 19(4): e0296989.
[31] WELTE T, KIM I S, TIAN L, et al. Oncogenic mTOR signalling recruits myeloid-derived suppressor cells to promote tumour initiation[J]. Nat Cell Biol, 2016, 18(6): 632-644.
[32] KUMAR S, WILKES D W, SAMUEL N, et al. ΔNp63-driven recruitment of myeloid-derived suppressor cells promotes metastasis in triple-negative breast cancer[J]. J Clin Invest, 2018, 128(11): 5095-5109.



 下载:
下载: