Impact of Hepatic-Intestinal First-Pass Effect on the Bioavailability of Schizandrin in Rats
-
摘要:
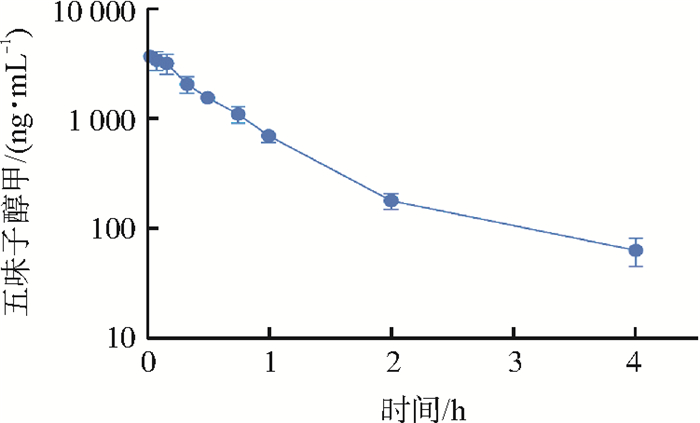
目的 以整体动物和肝肠首过代谢动物模型, 考察五味子主要活性成分五味子醇甲在体内外的处置过程, 探讨五味子醇甲低生物利用度的原因, 为五味子的现代化开发提供必要的数据支撑。 方法 首先研究不同剂量的五味子醇甲在整体动物(大鼠)体内的药动学过程; 其后借助颈静脉和幽门静脉插管的首过代谢模型, 研究肝脏、肠道在五味子醇甲体内转化过程中的作用以及对其生物利用度的影响。 结果 在清醒大鼠体内, 分别灌胃(i.g)给予10、20、50 mg · kg-1五味子醇甲后, 五味子醇甲表现为吸收快(Tmax, 0.37、0.44、0.33 h)、体内平均停留时间短(MRTlast, 1.74、1.65、1.27 h)、生物利用度较低(F, 12.0%, 11.0%, 9.35%)的药动学特性; 经i.g和十二指肠穿刺(i.d)给予20 mg · kg-1五味子醇甲的血药浓度-时间曲线下面积相近(AUC0-4 h,467.98 h · ng · mL-1 vs 469.03 h · ng · mL-1), 说明胃部首过效应对其生物利用度影响较小[胃利用度(FG)接近100%]; 经i.d给予20 mg · kg-1五味子醇甲后, 幽门静脉血中五味子醇甲的暴露量显著高于颈静脉中的暴露量(1 648.08 h · ng · mL-1 vs 469.03 h · ng · mL-1, P < 0.05), 以此估算肠道发生代谢的部分为78.47%;幽门静脉注射(i.p.v)给药后经颈静脉采血,五味子醇甲的系统暴露量低于静脉注射(i.v)给药后经颈静脉采血的系统暴露量(1 960.22 h · ng · mL-1 vs 2 547.79 h · ng · mL-1), 以此估算五味子醇甲摄取入肝脏发生代谢的部分为23.06%;综合肝脏利用度(Fh, 76.94%=1-23.06%)、肠道利用度(Fa × Fg, 21.53%=1-78.47%), 估算五味子醇甲的绝对生物利用度(Ft)为16.57%, 与i.g给药经颈静脉采血后计算的生物利用度(18.33%)接近; 在体外肝、肠微粒体体系中, 五味子醇甲发生明显的NADPH依赖的代谢。 结论 肝肠首过代谢在很大程度上影响五味子醇甲的生物利用度, 而肠道代谢对五味子醇甲的首过代谢贡献程度更大, 对其绝对生物利用度的影响更大。 Abstract:OBJECTIVES The pharmacokinetic analysis of schizandrin in rats were performed to investigate the potential impact of intestinal-hepatic first-pass effect on the low bioavailability of schizandrin from Schizandra sinensis Baill. METHODS Firstly, the pharmacokinetic assay was carried out in rats following intravenous (i.v) or intragastric (i.g) administration at different dose levels (10, 20, 50 mg · kg-1). Secondly, the jugular vein or pyloric vein cannulated rats model was established to study the specific role of intestine and liver on the schizandrin. RESULTS Schizandrin was rapidly absorbed (Tmax, 0.37, 0.44, 0.33 h), quickly eliminated with short mean resident time (MRTlast, 1.74, 1.65, 1.27 h) and low bioavailability (12.0%, 11.0%, 9.35%) in conscious rats treated with i.g administration 10, 20, 50 mg · kg-1 of schizandrin. The systemic exposure to schizandrin was comparable (AUC0-t, 467.98 vs 469.03 h · ng · mL-1) after i.g or intraduodenal (i.d) puncture administration at 20 mg · kg-1. This indicated the gastric effect to the metabolism of schizandrin was minor. Following i.d administration of schizandrin at 20 mg · kg-1, the pre-systemic exposure to schizandrin in pyloric vein was higher than that in jugular vein (AUC0-t, 1 648.08 vs 469.03 h · ng · mL-1). The calculated intestinal metabolism was estimated at 78.47%; After intravenous administration via portal vein at 10 mg · kg-1, the systemic exposure in jugular vein was a bit lower than that following intravenous via jugular vein at identical dose (AUC0-t, 1 960.22 vs 2 547.79 h · ng · mL-1), indicating the hepatic metabolism occupied 23.06%. Comprehensive consideration of intestinal (Fa × Fg, 21.53%) and hepatic (Fh, 76.94%) availability, the total bioavailability was estimated as 16.57% in cannulated rats, which was close to the value (18.33%) calculated from the i.g and i.v administration in anaesthetic rats. In the intestinal and hepatic microsomes incubation system, schizandrin was extensively degraded in the presence of NADPH. CONCLUSIONS The intestinal-hepatic first-pass effect largely determines the bioavailability of schizandrin, while the intestine contributes in a larger extent. -
表 1 大鼠血浆中4个浓度水平五味子醇甲批内和批间精密度、准确度结果(x±s)
Table 1. Intra-batch and inter-batch precision and accuracy of schizandrin in rat plasma at LLOQ and three QC levels (x±s)
理论值/(ng·mL-1) 批内(n=6) 批间(n=18) 测定值/(ng·mL-1) 精密度/% 准确度/% 测定值/(ng·mL-1) 精密度/% 准确度/% 1 0.88±0.02 2.79 88.2 0.96±0.06 6.18 96.0 2 1.97±0.08 4.32 98.4 1.86±0.06 3.10 93.0 50 46.32±1.25 2.71 92.6 49.19±2.31 4.69 98.4 800 775.50±11.49 1.48 96.9 782.80±24.70 3.16 97.9 表 2 大鼠血浆中五味子醇甲的基质效应、回收率以及不同条件下的稳定性研究(x±s,n=6)
Table 2. Matrix effect, recovery assay of schizandrin at three QC levels and stability investigation under different conditions at low and high QC levels in rat plasma (x±s,n=6)
理论值/(ng·mL-1) 基质效应/% 回收率/% 处理前稳定性 处理后稳定性 长期冷冻稳定性 冻融稳定性 2 101.43±13.14 87.12±2.16 1.92±0.05 1.88±0.18 1.75±0.11 1.82±0.07 50 98.40±6.38 94.27±4.05 — — — — 800 102.74±8.78 90.77±3.61 755.80±12.36 753.10±18.98 746.20±32.65 777.64±29.51 注: “—”表示此项目未考察。 表 3 大鼠i.v给予10 mg · kg-1, i.g给予10、20、50 mg · kg-1五味子醇甲的主要药动学参数(x±s,n=4)
Table 3. The pharmacokinetic parameters of schizandrin in rats after i.v administration of 10 mg · kg-1 and i.g administration of 10, 20, 50 mg · kg-1 (x±s, n=4)
药动学参数 i.v i.g 10 mg·kg-1 10 mg·kg-1 20 mg·kg-1 50 mg·kg-1 Tmax/h — 0.37±0.16 0.44±0.21 0.33±0.14 Cmax/(ng·mL-1) — 148.50±47.11 258.07±100.83 961.68±158.49 AUC0-4 h/(h·ng·mL-1) 2 533.74±241.50 303.66±87.47 559.24±208.54 1 185.20±327.75 t1/2/h 0.72±0.05 2.35±0.99 3.70±1.01 1.71±0.61 #CL/(L·h-1·kg-1) 3.87±0.32 21.93±5.91 21.88±9.51 28.81±5.16 #Vz/(L·kg-1) 4.04±0.54 70.73±22.50 108.11±32.39 73.35±35.24 MRTlast/h 0.71±0.09 1.74±0.09 1.65±0.10 1.27±0.07 F/% — 12.0 11.0 9.35 注: “—”表示参数未计算; #i.g给药的参数为CL/F和Vz/F。 表 4 大鼠i.g和i.d给予20 mg · kg-1五味子醇甲后颈静脉和幽门静脉血中五味子醇甲的主要药动学参数(x±s,n=4)
Table 4. The pharmacokinetic parameters of schizandrin in jugular vein and pyloric vein after i.g and i.d administration of 20 mg · kg-1 (x±s, n=4)
药动学参数 i.g i.d 颈静脉采血 颈静脉采血 幽门静脉采血 Tmax/h 0.25±0.17 0.17±0.00 0.71±0.34 Cmax/(ng·mL-1) 214.73±75.36 344.63±50.49 867.08±260.88* AUC0-4 h/(h·ng·mL-1) 467.98±147.76 469.03±31.01 1 648.08±794.15* t1/2/h 3.23±0.87 1.84±0.52 1.03±0.18 #CL/(L·h-1·kg-1) 26.41±9.04 30.03±5.22 13.43±6.36 #Vz/(L·kg-1) 117.41±39.58 78.80±22.64 18.96±7.17 MRTlast/h 1.65±0.10 1.25±0.28 1.36±0.12 F/% 18.33 — — FG/% 100.2 Fa×Fg/% 21.53 注: “—”表示参数未计算; #i.g给药的参数为CL/F和Vz/F; 与颈静脉采血组比较, *P < 0.05。 表 5 大鼠i.v和i.p.v给予10 mg · kg-1五味子醇甲的主要药动学参数(x±s,n=4)
Table 5. The pharmacokinetic parameters of schizandrin in rats after i.v and i.p.v administration of 10 mg · kg-1 (x±s, n=4)
药动学参数 i.v i.p.v Tmax/h — 0.17±0.00 Cmax/(ng·mL-1) — 2 745.42±78.26 AUC0-4 h/(h·ng·mL-1) 2 547.79±377.05 1 960.22±642.00 t1/2/h 0.61±0.15 0.78±0.34 #CL/(L·h-1·kg-1) 3.69±0.25 4.43±0.55 #Vz/(L·kg-1) 3.22±0.72 4.94±2.12 MRTlast/h 0.61±0.20 0.72±0.35 Fh/% 76.94 注: “—”表示参数未计算。 表 6 五味子醇甲在肝、肠微粒体体系中药动学参数(n=3)
Table 6. The in vitro metabolic parameters of schizandrin in the hepatic and intestinal microsomes system (n=3)
体系 药动学参数 1 2 3 s 肝微粒体 k/min-1 0.045 3 0.042 5 0.048 1 0.045 3 0.002 8 t1/2/min 15.3 16.3 14.4 15.4 1.0 CLint/(mL·min-1·mg-1) 0.090 6 0.084 9 0.096 1 0.090 5 0.005 6 肠微粒体 k/min-1 0.016 3 0.012 9 0.013 5 0.014 2 0.001 8 t1/2/min 42.5 53.6 51.4 49.2 5.9 CLint/(mL·min-1·mg-1) 0.032 7 0.025 8 0.027 0 0.028 5 0.003 6 -
[1] LI CL, CHENG YY, HSIEH CH, et al. Pharmacokinetics of schizandrin and its pharmaceutical products assessed using a validated LC-MS/MS method[J]. Molecules, 2018, 23(1): 173. doi: 10.3390/molecules23010173 [2] 邢楠楠, 屈怀东, 任伟超, 等. 五味子主要化学成分及现代药理作用研究进展[J]. 中国实验方剂学杂志, 2021, 27(15): 210-228. https://www.cnki.com.cn/Article/CJFDTOTAL-ZSFX202115032.htmXING NN, QU HD, REN WC, et al. Main chemical constituents and modern pharmacological action of Schisandrae Chinensis Fructus: A review[J]. Chin J Exp Tradit Med Form, 2021, 27(15): 210-228. https://www.cnki.com.cn/Article/CJFDTOTAL-ZSFX202115032.htm [3] 国家药典委员会. 中华人民共和国药典: 一部[M]. 北京: 中国医药科技出版社, 2020: 96.National Pharmacopoeia Committee. Pharmacopoeia of People's Republic of China: Ⅰ[M]. Beijing: China medical science press, 2020: 96. [4] WU XR, ZHOU Y, YIN FZ, et al. Comparative pharmacokinetics and tissue distribution of schisandrin, deoxyschisandrin and schisandrin B in rats after combining acupuncture and herb medicine (schisandra chinensis)[J]. Biomed Chromatogr, 2014, 28(8): 1075-1083. doi: 10.1002/bmc.3122 [5] CAO YF, ZHANG YY, LI J, et al. CYP3A catalyses schizandrin biotransformation in human, minipig and rat liver microsomes[J]. Xenobiotica, 2010, 40(1): 38-47. doi: 10.3109/00498250903366052 [6] LIANG Y, HAO HP, XIE L, et al. Development of a systematic approach to identify metabolites for herbal homologs based on liquid chromatography hybrid ion trap time-of-flight mass spectrometry: Gender-related difference in metabolism of Schisandra lignans in rats[J]. Drug Metab Dispos, 2010, 38(10): 1747-1759. doi: 10.1124/dmd.110.033373 [7] XU MJ, WANG GJ, XIE HT, et al. Determination of schizandrin in rat plasma by high-performance liquid chromatography-mass spectrometry and its application in rat pharmacokinetic studies[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2005, 828(1/2): 55-61. [8] 许美娟, 王广基, 谢海棠, 等. 五味子醇甲在大鼠肝微粒体内的代谢动力学和性别差异[J]. 药学学报, 2007, 42(7): 730-734. doi: 10.3321/j.issn:0513-4870.2007.07.008XU MJ, WANG GJ, XIE HT, et al. Enzyme kinetics of schizandrin metabolism and sex differences in rat liver microsomes[J]. Acta Pharm Sin, 2007, 42(7): 730-734. doi: 10.3321/j.issn:0513-4870.2007.07.008 [9] SHIN JH, CHOI KY, KIM YC, et al. Dose-dependent pharmacokinetics of itraconazole after intravenous or oral administration to rats: Intestinal first-pass effect[J]. Antimicrob Agents Chemother, 2004, 48(5): 1756-1762. doi: 10.1128/AAC.48.5.1756-1762.2004 [10] QIU ZX, LI N, SONG L, et al. Contributions of intestine and plasma to the presystemic bioconversion of vicagrel, an acetate of clopidogrel[J]. Pharm Res, 2014, 31(1): 238-251. -




 下载:
下载: